提醒成功

研究MMP9表达:抗体选择与实验方案
发布时间:2026-02-02 09:37:23基质金属蛋白酶9(MMP9)作为细胞外基质重塑的核心分子,其表达水平与定位特征的精准解析,是开展机制研究、疾病标志物筛选及药物研发的基础。抗体作为MMP9表达检测的核心工具,其质量优劣决定实验数据的可靠性与结论的科学性。实验方案的合理设计则为抗体效能发挥、结果精准度提供保障。精准筛选适配抗体、构建严谨实验体系,是推动MMP9相关研究走向深入的关键前提。
一、MMP9抗体选择的核心维度
(一)特异性验证:筑牢精准检测根基
特异性是抗体的核心属性,指其精准识别MMP9特定表位并排除同源蛋白干扰的能力。筛选时需重点核查抗体针对MMP9的识别区域,明确其对催化结构域、铰链区或羧基末端结构域的结合特异性,同时确认对MMP9潜伏态与活性态的识别能力。需严格排查与MMP家族其他成员(MMP1、MMP2等)的交叉反应,通过无MMP9表达的阴性样本孵育实验,排除非特异性结合引发的假阳性信号。
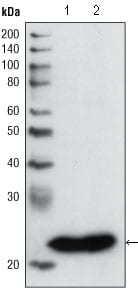
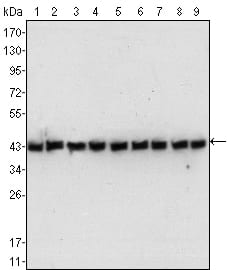
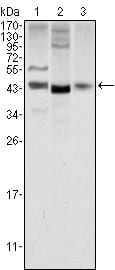
产品技术资料中的验证数据是特异性评估的重要依据。蛋白质印迹(WB)验证需关注条带分子量与理论值的一致性,确保条带单一、背景洁净;免疫组织化学(IHC)验证需确认阳性信号定位准确,无弥散性背景干扰。同行评议文献中该抗体的引用情况,可作为特异性与可靠性的补充佐证。
(二)应用兼容性:匹配实验技术需求
不同实验技术对抗体的性能要求存在差异,抗体应用场景的预验证是实验成功的前提。需根据研究目的明确检测技术,针对性筛选经对应技术验证的抗体。WB实验需选择能有效识别内源性或外源性MMP9的抗体,确保在蛋白分离与转膜后仍可稳定结合靶标;IHC实验需关注抗体对石蜡切片或冰冻切片的穿透能力,适配样本固定与抗原修复方式。
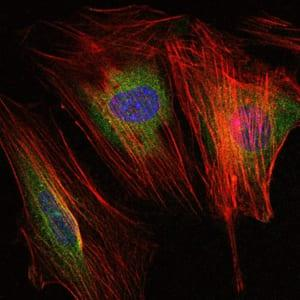
酶联免疫吸附实验(ELISA)需选用亲和力强、灵敏度高的抗体,满足定量检测需求;免疫荧光(IF)实验则需确认抗体与荧光二抗的兼容性能,保障亚细胞定位分析的信号清晰度。未在目标技术中验证的抗体,即便在其他场景表现优良,也不宜直接选用。
(三)性能稳定性与储存适配性
抗体稳定性影响实验可重复性与成本控制。需核查抗体在规定储存条件下的活性衰减速率,-20℃长期储存与4℃短期储存的性能维持能力,以及室温放置时的稳定性表现。批间变异系数是关键评估指标,需确保不同生产批次抗体的亲和力、特异性一致,避免批次差异导致实验数据偏移。
样本处理方式需与抗体特性适配。针对甲醛固定石蜡包埋样本,需选择支持对应抗原修复方法的抗体;仅适用于冰冻切片的抗体,不可用于石蜡切片检测。抗体稀释液需遵循厂家推荐,避免使用PBS或纯水简单稀释,防止影响结合活性。
二、MMP9表达检测实验方案设计
(一)实验前准备:优化基础条件
样本处理需兼顾完整性与靶标保留。细胞样本裂解需选用适配缓冲液,添加蛋白酶抑制剂防止MMP9降解;组织样本需根据类型选择合适固定方式,石蜡切片需严格控制脱蜡、抗原修复流程,避免表位破坏。抗体使用前需根据单次用量分装,避免反复冻融导致活性衰减,取用过程严格无菌操作,防止污染降解。
抗体浓度优化是提升信噪比的关键。厂家推荐浓度仅作为参考,需通过梯度稀释实验,结合样本中MMP9表达丰度,确定各实验技术的最佳稀释比例。WB实验可设置1:500至1:2000梯度,IHC实验设置1:200至1:1000梯度,筛选条带清晰、背景最低或阳性信号最特异的浓度。
(二)核心实验流程规范
WB实验需严格控制电泳、转膜参数,确保蛋白分离完全、转膜效率均一。孵育过程中,4℃过夜孵育可提升抗体结合特异性,室温孵育需精准控制时间。显影前需充分洗涤,去除未结合抗体,同时设置内参(GAPDH、β-Actin)校准上样量与转膜效果。
IHC实验需注重封闭步骤,用5%脱脂奶或BSA封闭非特异性结合位点。孵育抗体时需控制液量,避免样本干燥。显色过程需实时观察,及时终止反应防止信号过强或弥散。IF实验需选择适配的荧光二抗,控制孵育温度与时间,避光操作以保护荧光信号。
ELISA实验需严格遵循试剂盒说明书,控制包被、封闭、孵育、显色各步骤时间与温度一致性。标准曲线构建需设置足够梯度,确保定量范围覆盖样本预期浓度,同时进行复孔检测减少误差。
(三)对照体系构建与结果验证
完整对照体系是实验可靠性的保障。阳性对照选用已知高表达MMP9的细胞或组织样本,验证实验体系有效性;阴性对照采用MMP9敲低或敲除样本,确认抗体特异性;空白对照仅加入二抗,排除非特异性结合干扰。
结果分析需理性判读。WB实验若出现多条带,需结合分子量与敲低实验区分特异性条带与异构体、降解产物;无条带时需先排查实验流程,再质疑抗体效能。IHC结果需关注阳性信号定位与组织学特征的关联性,避免误判非特异性染色。所有实验需至少重复三次,确保数据可重复。
三、实验质量控制关键要点
实验全过程需强化质量管控,样本处理、抗体孵育、洗涤、显色等各环节均需保持操作一致性。仪器设备需定期校准,电泳仪、酶标仪、显微镜等性能稳定是数据精准的前提。试剂需在有效期内使用,不同批次试剂需进行预实验,确认性能一致。
特异性验证需贯穿实验全程,可通过肽段竞争实验进一步确认抗体特异性——用过量MMP9抗原肽段与抗体预先孵育,若信号显著减弱则证明结合特异性。对关键结果,建议采用两种不同表位的抗体交叉验证,提升结论可靠性。
MMP9表达研究的严谨性,根植于抗体选择的精准把控与实验方案的科学设计。抗体筛选需兼顾特异性、兼容性与稳定性,实验设计需强化对照体系与流程规范,能减少干扰因素,获取真实可靠的实验数据。












 微信/QQ登录
微信/QQ登录


 首页
首页