提醒成功

GPC3抗体开发技术
发布时间:2025-12-17 13:52:23糖基磷脂酰肌醇锚定蛋白3(GPC3)作为一种细胞膜表面糖蛋白,在正常组织中表达受限,而在多种恶性肿瘤中呈现特异性高表达,其表达水平与肿瘤发生发展进程密切相关。这种特异性表达特征,使GPC3成为肿瘤诊断与治疗领域的重要靶点。针对GPC3的抗体开发,旨在利用抗体的特异性结合能力,实现对肿瘤细胞的精准识别与干预,为肿瘤治疗提供新的技术方向。以下将对GPC3抗体开发技术进行梳理与解析。
GPC3靶点的特征解析与抗体开发前提
GPC3的分子结构决定其作为抗体靶点的可行性。该蛋白由氨基端信号肽、核心蛋白结构域、糖基化修饰区域及羧基端锚定结构组成,其中核心蛋白结构域中的特定氨基酸序列构成抗原表位,是抗体特异性结合的关键位点。其糖基化修饰程度在正常组织与肿瘤组织中存在显著差异,这种差异为抗体的特异性识别提供了结构基础。
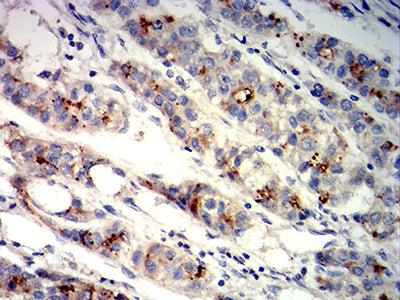
开展GPC3抗体开发前,需完成靶点的精准表征。通过基因克隆技术获取GPC3全长及不同结构域的基因序列,构建重组表达载体后,在合适的宿主细胞中进行表达纯化,获得高纯度的重组GPC3蛋白。借助X射线晶体衍射、核磁共振等技术解析GPC3的三维结构,明确抗原表位的空间构象;通过免疫组化、流式细胞术等方法验证GPC3在不同组织中的表达谱,确保靶点的特异性与有效性。这些前期工作为后续抗体筛选与优化提供可靠的靶点基础。
GPC3抗体的筛选策略与技术体系
抗体筛选是获取特异性GPC3抗体的核心环节,需建立高效的筛选体系。杂交瘤技术是传统的抗体筛选方法,将免疫后的小鼠脾细胞与骨髓瘤细胞融合,构建杂交瘤细胞库。利用酶联免疫吸附试验(ELISA)对细胞培养上清进行初筛,检测与重组GPC3蛋白的结合能力;通过流式细胞术进行复筛,验证对肿瘤细胞表面天然GPC3蛋白的识别能力,获得分泌特异性抗体的杂交瘤细胞株。
噬菌体展示技术为全人源GPC3抗体的筛选提供了新途径。构建人源抗体库后,以重组GPC3蛋白为靶点进行多轮淘选,富集能特异性结合GPC3的噬菌体克隆。对筛选得到的阳性克隆进行测序分析,获得抗体可变区基因序列,通过基因工程技术构建完整的人源抗体表达载体,在哺乳动物细胞中进行表达纯化。该技术可避免鼠源抗体的免疫原性问题,提升抗体的临床应用潜力。
GPC3抗体的优化与功能验证
筛选获得的初始抗体需进行针对性优化,提升其生物学性能。抗体亲和力优化可通过定点突变、链改组等技术对抗体可变区进行改造,增强与GPC3的结合能力。抗体稳定性优化则聚焦于恒定区序列修饰,提升抗体在体外储存及体内循环过程中的稳定性,减少降解风险。同时,通过Fc段工程改造可调节抗体的效应功能,如增强抗体依赖的细胞介导的细胞毒性(ADCC)、补体依赖的细胞毒性(CDC)等,提升对肿瘤细胞的杀伤效果。
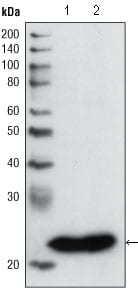
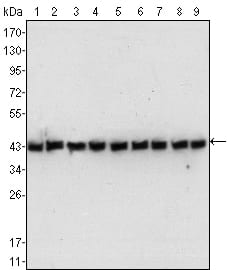
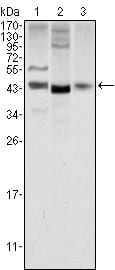
功能验证是评估GPC3抗体性能的关键步骤。体外实验中,通过细胞增殖抑制试验、凋亡检测等方法,验证抗体对肿瘤细胞生长的抑制作用;通过免疫沉淀、Western Blot等技术,明确抗体与GPC3的结合特异性。体内实验则利用肿瘤异种移植模型,检测抗体在动物体内的药代动力学特征,评估其对肿瘤生长的抑制效果及安全性,为抗体的临床转化提供数据支撑。
GPC3抗体开发技术以靶点的特异性特征为基础,通过筛选体系的构建、抗体的优化及功能验证等关键环节,实现特异性抗体的制备。杂交瘤技术与噬菌体展示技术的协同应用,为不同来源的GPC3抗体开发提供技术支撑;抗体优化技术的不断革新,提升了抗体的生物学性能与临床应用价值。












 微信/QQ登录
微信/QQ登录


 首页
首页